Perspectivas del mercado de tratamientos para enfermedades raras:
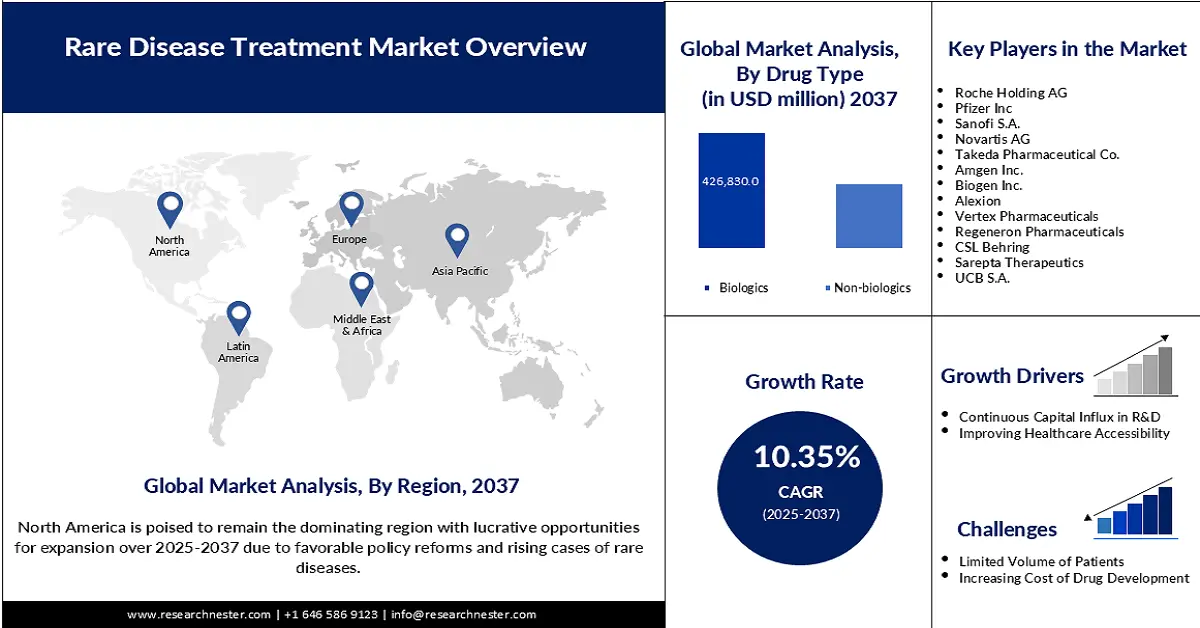
El mercado de tratamientos para enfermedades raras alcanzó los 232.200 millones de dólares en 2024 y se estima que llegará a los 792.800 millones de dólares a finales de 2037, con una tasa de crecimiento anual compuesta (TCAC) del 10,35 % durante el período de previsión, es decir, de 2025 a 2037. En 2025, el tamaño del sector de tratamientos para enfermedades raras se estima en 243.100 millones de dólares.
El mercado mundial de tratamientos para enfermedades raras se caracteriza por un grupo de pacientes limitado pero diverso. Según la Comisión Mundial de Enfermedades Raras (GRDC), en 2024 más de 300 millones de personas en todo el mundo se verían afectadas por estas afecciones. En regiones clave como Estados Unidos, Japón y Europa, la población objetivo es reducida, pero la epidemiología acumulada sigue creciendo gracias a la mejora de la capacidad diagnóstica y la heredabilidad de las mutaciones genéticas. Como resultado, aproximadamente el 70 % de estas enfermedades se presentan en niños. La amplia gama de estas afecciones también impulsa la demanda en este sector, donde se identificaron más de 7000 tipos de enfermedades raras en todo el mundo hasta 2024, con un potencial de superar los 10 000 y 300 nuevas descripciones de enfermedades genéticas raras que se añaden cada año a las principales bases de datos.
Además, en su informe de 2022 del Instituto para la Revisión Clínica y Económica (ICER), que ofrece una perspectiva financiera sobre la fijación de precios por parte de las aseguradoras, se reveló que un precio anual de 100 000 USD para un medicamento huérfano, destinado a una población limitada de 10 000 pacientes con estas enfermedades, puede generar ingresos anuales de 1000 millones de USD. El informe también menciona que el costo total del tratamiento de estas afecciones por persona suele superar el millón de USD anuales, debido al elevado precio de los medicamentos huérfanos certificados y las terapias génicas y celulares . Estas cifras reflejan la inflación en los costos de productos y servicios para los usuarios finales y los consumidores, junto con las lucrativas oportunidades que ofrecen los medicamentos de alto precio.
Mercado de tratamientos para enfermedades raras: factores de crecimiento y desafíos
Factores de crecimiento
- Avances en el diagnóstico y la comprensión de las enfermedades: Según un artículo del Instituto Nacional de Salud (NIH) de 2025, el 80 % de las enfermedades raras se clasifican como genéticas, de las cuales el 70 % y el 3 % se manifiestan durante la infancia y el período neonatal, respectivamente. Esto demuestra la importancia del rápido crecimiento y los avances en la secuenciación del genoma como un factor clave de crecimiento en el mercado. En consonancia con esto, en 2022, la Biblioteca Nacional de Medicina (NLM) publicó un metaanálisis que destacó que las tasas de diagnóstico combinadas de la secuenciación del exoma completo (WES) y la secuenciación del genoma completo (WGS) fueron superiores a las de los métodos convencionales, con un 0,3 % y un 0,4 %, respectivamente, lo que abre nuevas posibilidades para casos previamente no tratados.
Ahorro de costes gracias a la secuenciación genómica rápida en la práctica clínica (2022)
País | Método de secuenciación | Resultados clave |
Australia | WES rápido | Ahorro de 408.090 USD gracias a la reducción de procedimientos y días de hospitalización. |
Hong Kong | WES rápido | Se redujeron 566 días de hospitalización y se ahorraron 1,03 millones de dólares. |
A NOSOTROS | WGS rápido | Ahorro neto de 128.555 USD gracias a la reducción de días de hospitalización. |
Fuente: NLM
- Aumento de las inversiones en I+D y ampliación de la cartera de productos : Tanto las organizaciones públicas como las privadas de todo el mundo están invirtiendo fuertemente en investigación exhaustiva para ampliar los campos de aplicación de sus carteras de productos existentes. Cada año, se destinan más de 10 000 millones de dólares exclusivamente a estos grupos en el mercado mundial del tratamiento de enfermedades raras. Por otro lado, el éxito comercial de las innovaciones derivadas de estos esfuerzos también está alcanzando hitos importantes. Como ejemplo, el lanzamiento de Attruby (acoramidis) para el tratamiento de la amiloidosis cardíaca por transtiretina (ATTR-CM) en noviembre de 2024 generó 36,7 millones de dólares en ventas para BridgeBio Pharma solo en el mercado estadounidense.
- Mayor apoyo de las autoridades gubernamentales : La reciente reforma de la gobernanza pública y de certificación garantiza el progreso futuro y una expansión sustancial para los fabricantes en el mercado mediante la asignación de subsidios, incentivos y aprobaciones aceleradas. Esto crea un entorno favorable para el sector, a la vez que evita pérdidas financieras y de valor de marca al ahorrar costos relacionados con los procesos de cumplimiento que consumen mucho tiempo y el vencimiento de patentes. Un hito importante en este sentido fue la autorización de más de 20 terapias génicas por parte de la FDA en los últimos años. Por ejemplo, en septiembre de 2024, Sanofi obtuvo la designación de medicamento huérfano (ODD) de la FDA para Dupixent, un fármaco para el tratamiento del penfigoide ampolloso.
Patrones demográficos en los principales escenarios del mercado de tratamientos para enfermedades raras
Panorama general de la incidencia y prevalencia de enfermedades raras (ER) en los EE. UU. (2023)
Región/Categoría | Tasa de prevalencia estimada |
En general, EE. UU. | 1 de cada 10 personas |
Massachusetts | Afecta a aproximadamente el 10% de la población |
Estado de Washington | Entre 700 y 800 mil personas adquieren RD |
Fibrosis quística | 0,06% |
Síndrome de Ehlers-Danlos | 0,15% |
Síndrome de Turner | 0,02% |
Fuente: FDA, DOH Washington e ISPOR
Proyectos de desarrollo recientes/en curso relacionados con el mercado de tratamientos para enfermedades raras
Ensayos clínicos actuales/recientes/en curso sobre fármacos para enfermedades reumáticas
Nombre del medicamento | Indicación | Patrocinador | Fase de estudio | Notas clave | Cronología |
Venglustat | Enfermedad de Gaucher tipo 3 | Sanofi Genzyme | Fase 3 | Terapia de reducción de sustrato oral; evaluación de la seguridad a largo plazo | Activo (Finaliza en 2026) |
Hurlerase (vestronidasa alfa) | Mucopolisacaridosis VII | Ultragenyx | Fase 4 | Terapia de reemplazo enzimático en pacientes pediátricos | En curso desde 2023 |
Luxturna | Enfermedad retiniana hereditaria | Spark Therapeutics | Seguimiento/Fase 4 | Terapia génica para la distrofia retiniana asociada a la mutación RPE65 | Seguimiento a largo plazo en curso |
Elivaldogene autotemcel | Leucodistrofia metacromática | Terapéutica de Orchard | Fase 3 | Terapia génica autóloga, infusión única | Activo (Finalización en 2025) |
Zynteglo | Beta-talasemia | Biografía de Bluebird | Fase 3/Aprobado | Terapia génica, transducción de células madre autólogas | Estudios aprobados y en curso |
Roctaviano | Hemofilia A | BioMarin | Fase 3 | Terapia génica para la deficiencia del factor VIII | Activo (Finaliza en 2026) |
Amondys 45 | Distrofia muscular de Duchenne | Terapéutica Sarepta | Fase 3 | Oligonucleótido antisentido de omisión de exón | En curso (2023-2025) |
Olipudasa alfa | Deficiencia de esfingomielinasa ácida | Sanofi Genzyme | Fase 3 | Terapia de reemplazo enzimático para la enfermedad de Niemann-Pick | Recientemente finalizado |
Libmeldy | Leucodistrofia metacromática | Terapéutica de Orchard | Fase 2/3 | Terapia génica; aprobada por la EMA, pendiente de aprobación en EE. UU. | Registro en curso |
Fuente: Clinicaltrials.gov
Desafíos
- Limitaciones de infraestructura y accesibilidad: Varias economías, en particular las regiones desatendidas, enfrentan obstáculos para acceder a productos y servicios adecuados en el mercado. La falta de recursos suficientes, infraestructura, protocolos de estandarización y capacidades de diagnóstico genera deficiencias en el acceso de los pacientes, lo que en última instancia limita la adopción de este sector. En consonancia con este problema, el informe del ICER reveló que el 90 % de los casos afectados carecían de tratamientos específicos aprobados por la FDA para la enfermedad hasta 2022.
- Altas presiones de las aseguradoras sobre los precios : Un estudio de la NLM de 2024 clasificó a Zolgensma para el tratamiento de la atrofia muscular espinal (AME) como un tratamiento de alto costo debido a su precio de 2,1 millones de dólares por dosis. En consecuencia, una proporción considerable de aseguradoras tiende a imponer controles estrictos sobre precios tan elevados y, a menudo, excluye estas opciones de sus planes de cobertura de reembolso. Esto no solo reduce la accesibilidad y la adopción de tratamientos para enfermedades raras, sino que también disminuye el margen de rentabilidad para los fabricantes de terapias avanzadas.
Tamaño y pronóstico del mercado de tratamientos para enfermedades raras:
| Atributo del informe | Detalles |
|---|---|
|
Año base |
2024 |
|
Año de pronóstico |
2025-2037 |
|
CAGR |
10,35% |
|
Tamaño del mercado del año base (2024) |
232.200 millones de dólares |
|
Previsión del tamaño del mercado para el año 2037 |
792.8 mil millones de dólares |
|
Alcance regional |
|
Segmentación del mercado de tratamientos para enfermedades raras:
Análisis de segmentos por tipo de fármaco
Se prevé que el segmento de productos biológicos represente la mayor cuota de mercado, con un 53,8%, durante el periodo analizado. Este liderazgo se atribuye principalmente a la creciente popularidad de la medicina de precisión en el tratamiento de enfermedades difíciles de tratar. Además, como parte de esta categoría, los biosimilares se están convirtiendo en candidatos idóneos para programas gubernamentales que promueven la accesibilidad económica, lo que los convierte en activos ampliamente aceptados y comercializados en este sector. Asimismo, la reputación del segmento como referente en cumplimiento normativo se evidencia con la aprobación por parte de la FDA de Bkemv y Soliris como biosimilares intercambiables para enfermedades raras en mayo de 2024.
Análisis de segmentos de enfermedades
Se prevé que el segmento de trastornos hematológicos en el mercado ostente la mayor cuota de ingresos, con un 45,4%, entre 2025 y 2037. La alta prevalencia y las elevadas tasas de mortalidad de estas enfermedades, como la anemia falciforme, la hemofilia y la hemoglobinuria paroxística nocturna, especialmente entre los niños, son los principales factores que impulsan este dominio. Según un estudio de la Carga Mundial de Morbilidad (GBD), el número total de nacimientos de bebés y de personas que viven con anemia falciforme aumentó un 13,7% y un 41,4%, respectivamente, en todo el mundo entre 2000 y 2021. Por otro lado, la eficacia clínicamente demostrada de las terapias génicas y celulares está atrayendo una mayor inversión de capital para el desarrollo de nuevos fármacos en esta área médica.
Análisis de segmentos de pacientes
Se prevé que el grupo de edad pediátrica sea el segmento de pacientes líder en el mercado para finales de 2037, con una cuota del 67,9 %. Según una publicación de 2023 del Journal of Pediatric Nursing, entre el 50 % y el 75 % de todas las enfermedades raras se producen en niños. Además, otro estudio de la NLM del mismo año reveló que las muertes por anemia falciforme en menores de 5 años ascendieron a 81 100 entre 2000 y 2021, una cifra superior a la mortalidad por otras causas. Estos datos ponen de manifiesto la concentración de la mayor parte de la actividad del sector en este segmento, consolidando así su posición de liderazgo.
Nuestro análisis exhaustivo del mercado incluye los siguientes segmentos:
Segmento | Subsegmento |
Tipo de medicamento |
|
Enfermedades |
|
Paciente |
|
Vía administrativa |
|
Canal de distribución |
|

Vishnu Nair
Jefe de Desarrollo Comercial GlobalPersonalice este informe según sus necesidades: conéctese con nuestro consultor para obtener información y opciones personalizadas.
Mercado de tratamientos para enfermedades raras: análisis regional
Perspectivas del mercado norteamericano
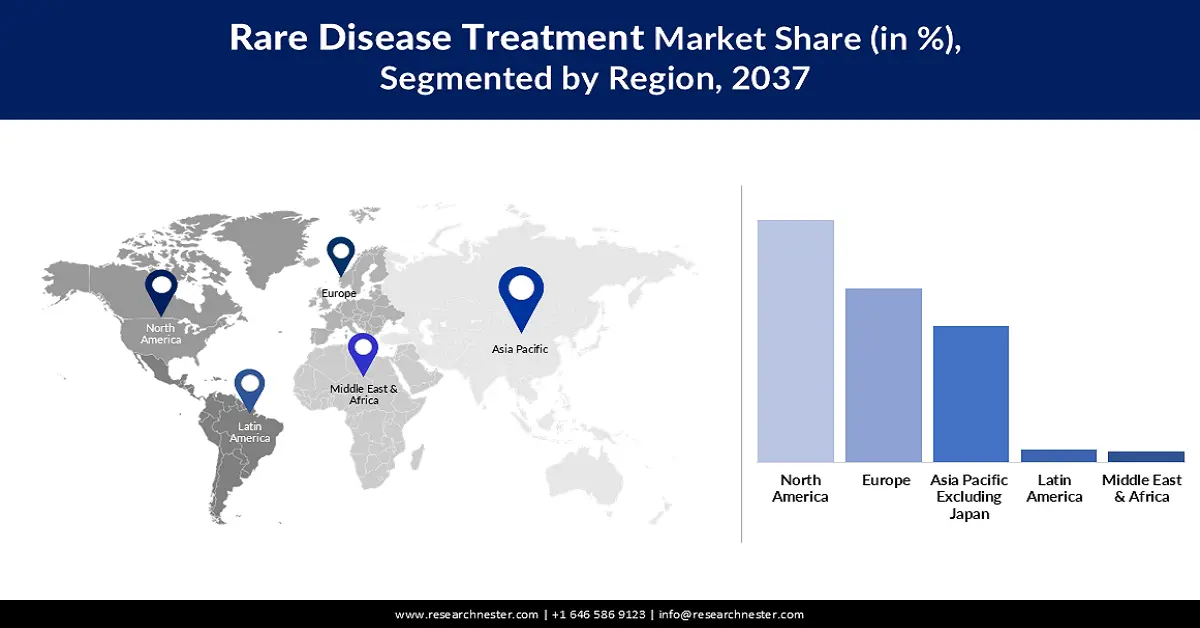
Se prevé que Norteamérica domine el mercado con una cuota del 57,6 % durante el periodo evaluado. La mayor incidencia de enfermedades raras en comparación con otras regiones del Pacífico es el principal factor de crecimiento en este ámbito. La presencia de empresas líderes y las políticas gubernamentales favorables también constituyen un activo importante para la región en este sector. Como prueba de dicho apoyo, un informe de la FDA de 2024 destacó los beneficios y el impacto positivo de la Ley de Medicamentos Huérfanos en el desarrollo futuro de fármacos para enfermedades raras en el mercado estadounidense. Esta ley permite una exención de hasta 3 millones de dólares en la tasa de usuario de medicamentos recetados y siete años de amplia exclusividad de mercado para los nuevos fármacos aprobados por la FDA.
El creciente número de pacientes en EE. UU. exige la expansión de la capacidad de desarrollo y fabricación en el mercado del tratamiento de enfermedades raras. Prueba de ello es el informe de la FDA de 2024, que indica que el número de personas con enfermedades raras alcanzó los 30 millones en el país. Además, EE. UU. cuenta con un sistema médico avanzado que ofrece la infraestructura necesaria para acceder a herramientas y servicios de diagnóstico de última generación, lo que impulsa la expansión en la región. Asimismo, la aprobación oportuna de productos, el surgimiento de terapias basadas en CRISPR y la alta concienciación pública en EE. UU. están impulsando el sector.
Aproximadamente 1 de cada 12 personas en Canadá padece una enfermedad rara, lo que genera una necesidad urgente de tratamientos eficaces y medidas preventivas. Por otro lado, para superar la brecha de acceso, en 2023 el gobierno canadiense lanzó la Estrategia Nacional para Medicamentos de Alto Costo para Enfermedades Raras, que subsidia la compra de medicamentos, garantizando así su asequibilidad para los pacientes afectados y la rentabilidad para los fabricantes. Además, los medicamentos disponibles en el mercado representan alrededor de una décima parte de las ventas farmacéuticas en Canadá, lo que refleja un entorno favorable.
Perspectivas del mercado de Asia Pacífico
Se prevé que el mercado de Asia Pacífico registre la mayor tasa de crecimiento anual compuesto (TCAC) del 11,5 % para finales de 2037. Este ritmo de crecimiento se atribuye principalmente al gran énfasis en la ampliación de la capacidad de atención para enfermedades raras y al aumento de las inversiones públicas y privadas en salud. En particular, en China, India, Vietnam e Indonesia, la creciente tendencia a producir el máximo volumen de productos biológicos está impulsando notablemente el sector en la región de Asia Pacífico. Además, la optimización de los ensayos clínicos y la actualización de los procesos regulatorios están permitiendo la comercialización masiva de opciones terapéuticas tempranas para combatir la mortalidad por progresión de la enfermedad.
Japón es uno de los centros de innovación más importantes y cuenta con una exigente base de consumidores en el mercado de Asia-Pacífico. El creciente énfasis del país en la medicina de precisión y su ambicioso objetivo de superar la escasez de medicamentos están impulsando la asignación de un importante presupuesto sanitario a este sector. Los esfuerzos del gobierno por fortalecer a este colectivo se evidencian en las políticas del Sistema de Medicamentos Huérfanos, que ofrece 10 años de exclusividad de mercado, subvenciones para I+D que cubren el 50 % de los costes de los ensayos clínicos y una revisión seis meses más rápida que la de los medicamentos convencionales.
En China , el mercado crece de forma constante gracias al aumento de casos de enfermedades raras y a la existencia de un sistema sanitario centralizado. Además, las mejoras en los procesos de adquisición de patentes durante los últimos años están atrayendo grandes inversiones y una mayor participación de empresas nacionales y extranjeras en este sector. Como prueba de ello, las reformas regulatorias de 2017 en China propiciaron el lanzamiento de más de 50 fármacos multinacionales para enfermedades raras, impulsadas por el aumento de las aprobaciones de medicamentos huérfanos en 2022, que pasaron de 3 anuales antes de la reforma a más de 30.
Oportunidades viables en paisajes clave
País | Notas clave |
Corea del Sur | Reembolso del 100% para 167 enfermedades raras designadas |
Japón | Se asignó el 4% del presupuesto nacional de salud a la investigación de enfermedades intratables. |
India | Una población de pacientes de 70 millones, con solo un 5% diagnosticados correctamente. |
Fuente: Informe de investigación de Nester
Perspectivas del mercado europeo
Se prevé que el mercado de tratamientos para enfermedades raras en Europa ocupe una posición destacada entre 2025 y 2037. Los marcos de reembolso bien estructurados y los incentivos regulatorios son los principales factores de crecimiento en este sector, impulsando la expansión constante de la región. Con 36 millones de pacientes con enfermedades raras, el panorama también favorece un entorno comercial atractivo para estos productos, según el informe de 2025 del Parlamento Europeo. Además, entre las iniciativas gubernamentales que benefician al mercado se incluye la creación de la Alianza Europea para la Investigación de Enfermedades Raras (ERDERA) en octubre de 2024, que financia la investigación en prevención, diagnóstico y tratamiento de enfermedades raras con 447,3 millones de dólares hasta 2031.
En Alemania , se prevé que el mercado lidere el territorio europeo gracias a su sólida infraestructura sanitaria, capaz de atender al creciente número de pacientes. El país cuenta además con una extensa red de centros especializados, como el ACHSE, que facilita el diagnóstico precoz, el tratamiento y la atención al paciente. Asimismo, con un creciente interés en el desarrollo de fármacos avanzados y productos biológicos de última generación, se espera que el país experimente un rápido crecimiento en este sector durante los próximos años.
El mercado de tratamientos para enfermedades raras en Francia está impulsado principalmente por la HAS y la asignación presupuestaria de solidaridad. Los esfuerzos a nivel nacional para fortalecer los centros sanitarios existentes para la intervención y el diagnóstico precoces también están generando un auge lucrativo en este campo. En los próximos años, se espera que el aumento de las inversiones públicas y privadas en terapias génicas y celulares transforme los proyectos en desarrollo en el país, atrayendo a más inversores internacionales que deseen invertir sus recursos en este ámbito.
Oportunidades viables para el mercado
Iniciativa | Notas clave | Cronología |
Redes Europeas de Referencia (ERN) | 1.619 centros especializados ubicados en 382 hospitales, para abordar enfermedades y afecciones raras, de baja prevalencia y complejas que requieren atención sanitaria altamente especializada. | 2017-2024 |
Acción Conjunta para la Integración de las Personas Mayores en los Sistemas Nacionales de Salud (JARDIN) | Recibió 17,6 millones de dólares del programa EU4Health y 4,4 millones de dólares de los Estados miembros de la UE para facilitar un mayor acceso de los pacientes. | 2024-2027 |
Sistema de Gestión Clínica de Pacientes 2.0 | La Comisión Europea puso en marcha una nueva plataforma informática para ofrecer un mejor apoyo a las Redes Europeas de Referencia (ERN), reduciendo la necesidad de que los pacientes se desplacen. | 2024 |
Fuente: Parlamento Europeo
Principales actores del mercado de tratamientos para enfermedades raras:
- Descripción general de la empresa
- Estrategia empresarial
- Ofertas de productos clave
- Desempeño financiero
- Indicadores clave de rendimiento
- Análisis de riesgos
- Desarrollo reciente
- Presencia regional
- Análisis FODA
El mercado mundial de tratamientos para enfermedades raras está altamente consolidado, con varios gigantes biofarmacéuticos como Pfizer, Roche, Takeda y Sanofi controlando una cuota de mercado considerable. Estas compañías se centran en fortalecer sus carteras en esta categoría mediante la adquisición de designaciones de medicamentos huérfanos, la innovación en terapia génica y celular, y la expansión estratégica en territorios regionales para mantener su dominio en la generación de ingresos netos en este sector. Por otro lado, varios actores clave de Asia Pacífico están debutando a través de biosimilares y colaboraciones público-privadas.
Aquí tienes una lista de los principales actores que operan en el mercado:
nombre de empresa | País | Participación en los ingresos (2037) |
Roche Holding AG | Suiza | 8,9% |
Novartis AG | Suiza | 8,1% |
Johnson & Johnson | A NOSOTROS | 6,8% |
Pfizer Inc. | A NOSOTROS | 6,5% |
Sanofi SA | Francia | 6,2% |
Compañía farmacéutica Takeda | Japón | xx% |
Amgen Inc. | A NOSOTROS | xx% |
Biogen Inc. | A NOSOTROS | xx% |
Alexion | A NOSOTROS | xx% |
Productos farmacéuticos Vertex | A NOSOTROS | xx% |
Productos farmacéuticos Regeneron | A NOSOTROS | xx% |
CSL Behring | Australia | xx% |
Terapéutica Sarepta | A NOSOTROS | xx% |
UCB SA | Bélgica | xx% |
Ipsen | Francia | xx% |
Chugai Pharmaceutical | Japón | xx% |
Kyowa Kirin | Japón | xx% |
Laboratorios del Dr. Reddy | India | xx% |
Productos biológicos de Samsung | Corea del Sur | xx% |
A continuación se detallan las áreas que cubre cada empresa en el mercado global:
Desarrollos Recientes
- En septiembre de 2025, Alexion anunció que Koselugo (selumetinib) obtuvo una recomendación de aprobación en la Unión Europea (UE) para el tratamiento de neurofibromas plexiformes (PN) sintomáticos e inoperables en pacientes adultos con neurofibromatosis tipo 1 (NF1).
- En junio de 2025, CSL Behring recibió la aprobación de la FDA para Andembry , el primer tratamiento profiláctico dirigido al factor XIIa para el angioedema hereditario (AEH), que ofrece una dosis mensual para pacientes de 12 años o más. Su novedoso mecanismo, respaldado por rigurosos ensayos clínicos, lo posiciona como una opción transformadora en un mercado competitivo.
- Report ID: 6667
- Published Date: Oct 06, 2025
- Report Format: PDF, PPT
- Explore una vista previa de las principales tendencias e ideas del mercado
- Revise tablas de datos de muestra y desgloses por segmento
- Experimente la calidad de nuestras representaciones visuales de datos
- Evalúe nuestra estructura de informe y metodología de investigación
- Obtenga una vista de la análisis del panorama competitivo
- Comprenda cómo se presentan las previsiones regionales
- Evalúe la profundidad del perfilado de empresas y análisis comparativo
- Vea cómo los insights accionables pueden respaldar su estrategia
Explore datos y análisis reales
Preguntas frecuentes (FAQ)
Tratamiento de enfermedades raras Alcance del informe de mercado
La muestra gratuita incluye el tamaño del mercado actual e histórico, tendencias de crecimiento, gráficos y tablas regionales, perfiles de empresas, previsiones por segmento y más.
Conéctate con nuestro experto




