抗核抗体检测市场展望:
2025年抗核抗体检测市场规模超过18.8亿美元,预计到2035年将达到65.5亿美元,在预测期内(即2026-2035年)的复合年增长率约为13.3%。2026年,抗核抗体检测的行业规模估计为21.1亿美元。

市场的增长可归因于自身免疫性疾病的患病率上升以及全球试剂租赁协议数量的增长。根据世界卫生组织 (WHO) 发布的一份报告,2017 年,全球有 900 万人患有 1 型糖尿病,而全球人口中约有 4.22 亿人患有某种类型的糖尿病。此外,全球每年有 150 万人死于糖尿病。自身免疫性疾病可能是遗传性的,也可能是后天获得的,会导致患者免疫系统受到抑制。免疫系统受抑制人群中病毒和细菌感染发病率增加,自身免疫性疾病的高风险预计将推动市场增长。
此外,预计在预测期内,人们对 ANA 检测的认识不断提高以及抗生素使用量的增加也将推动市场的增长。美国国家医学图书馆 (NLM) 2020 年发布的数据显示,全球共进行了 587,357 次 ANA 检测,而 437,966 名患者接受了 ANA 检测。在现代社会,科技和健康意识都在呈指数级增长。因此,所有这些因素都有望在预测期内推动市场的增长。此外,人们在医疗保健需求和基本医疗方面的支出能力不断增强,预计也将推动市场的增长。
关键 抗核抗体检测 市场洞察摘要:
区域亮点:
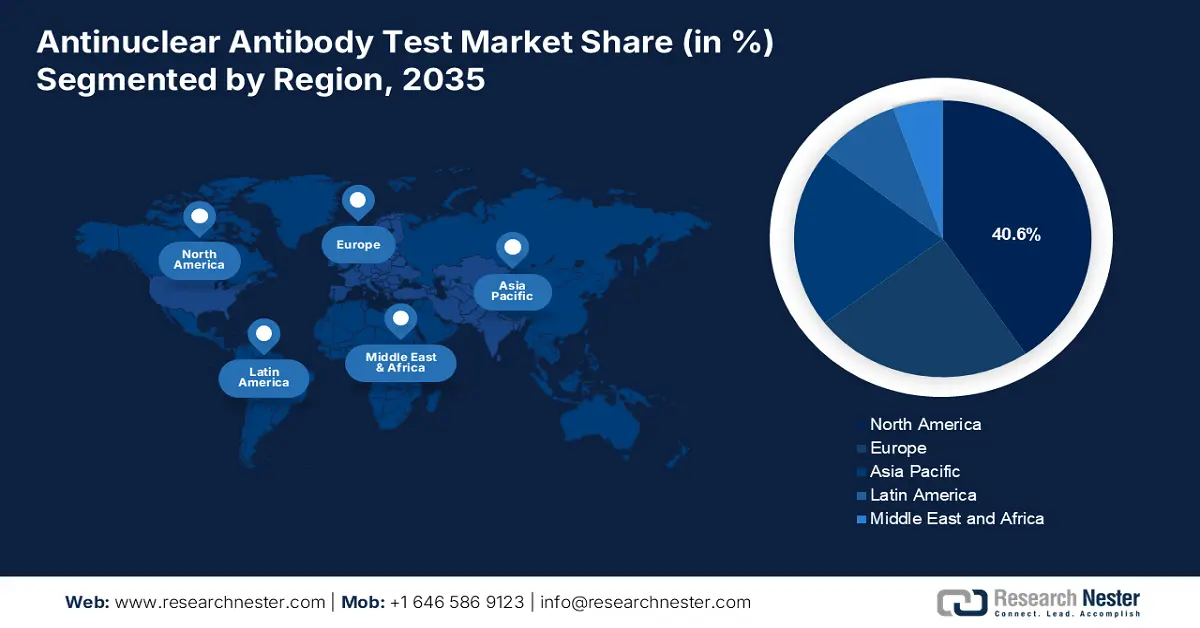
- 到2035年,北美抗核抗体检测市场将占据超过40.6%的市场份额,这得益于自身免疫性疾病患病率的上升和人口老龄化。
- 由于自身免疫性疾病病例的增加以及政府医疗保健举措的推动,亚太市场将在2026年至2035年期间快速增长。
细分市场洞察:
- 预计到 2035 年,抗核抗体检测市场中的检测试剂盒细分市场将占据相当大的份额,这得益于其在研究、远程医疗活动和生物制药试剂盒生产领域的应用日益增长。
- 预计到 2035 年,抗核抗体检测市场中的 ELISA 细分市场将占据显著的份额,这得益于其在治疗药物监测和自身免疫性疾病诊断领域的应用日益增长。
主要增长趋势:
- 全球人口自身免疫性疾病患病率上升
- 全球老年人口不断增长,免疫力下降
主要挑战:
- 缺乏熟练操作检测试剂盒的专业人员
- 诊断过程中存在错误风险,可能导致假阳性和假阴性结果
主要参与者:F. Hoffmann-La Roche Ltd.、ERBA Diagnostics, Inc.、Zeus Scientific Inc.、Trinity Biotech plc、Thermo Fisher Scientific Inc.、Bio-Rad Laboratories, Inc.、Immuno Concepts Inc.、Euroimmun Medizinische Labordiagnostika AG、Antibodies Incorporated、Becton, Dickinson and Company。
全球 抗核抗体检测 市场 预测与区域展望:
市场规模和增长预测:
- 2025年市场规模: 18.8亿美元
- 2026年市场规模: 21.1亿美元
- 预计市场规模:到 2035 年将达到 65.5 亿美元
- 增长预测:复合年增长率13.3%(2026-2035年)
主要区域动态:
- 最大的地区:北美(到 2035 年占比 40.6%)
- 增长最快的地区:亚太地区
- 主要国家:美国、德国、日本、英国、中国
- 新兴国家:中国、印度、巴西、墨西哥、韩国
Last updated on : 9 September, 2025
抗核抗体检测市场——增长动力与挑战
增长动力
全球人口自身免疫性疾病患病率不断上升——预计未来几年,患有自身免疫性疾病的人数将持续增长,推动市场增长。受多种环境因素的影响,全球自身免疫性疾病的发病率每年增长4%-10%。饮食习惯的改变、胆固醇和血糖水平的升高以及体力劳动的减少,共同推动着市场的增长。糖尿病、类风湿性关节炎和多发性硬化症患者数量的增加,也将在未来几年推动市场的增长。
全球老年人口不断增长,免疫力下降——预计到 2050 年,美国老年人口将超过 8500 万,在短短三十年内,老年人口将从目前的 4000 万增加一倍。
随着健康重要性的不断提高,医疗保健行业也随之扩大——根据观察,预计在未来五年(2022-2027 年)内,美国的国家医疗保健支出将增长 7%。
诊断实验室数量不断增加,疾病发病率不断上升——据估计,截至 2023 年,美国在全球拥有超过 25,000 个诊断和医疗实验室。
挑战
- 缺乏能够处理测试套件的熟练专业人员
- 诊断过程中的错误风险导致假阳性和假阴性结果
- 实验室设备价格高昂——用于抗核抗体测试的实验室设备通常价格昂贵,因此一些发达国家和发展中国家的小型实验室都无法负担得起。
抗核抗体测试市场规模和预测:
| 报告属性 | 详细信息 |
|---|---|
|
基准年 |
2025 |
|
预测期 |
2026-2035 |
|
复合年增长率 |
13.3% |
|
基准年市场规模(2025年) |
18.8亿美元 |
|
预测年度市场规模(2035年) |
65.5亿美元 |
|
区域范围 |
|
抗核抗体测试市场细分:
技术细分分析
到2035年,抗核抗体检测市场中的酶联免疫吸附试验(ELISA)预计将占据显著的收入份额,这得益于其在治疗药物监测中的应用,以及抗核抗体(ANA)在自身免疫性疾病中的应用日益增长。此外,ELISA的扩展形式是一种酶联免疫吸附试验,通常用于检测血液中的抗体。ELISA是一种检测患者体内是否存在抗体的检测方法,这些抗体是机体对被称为抗原的外来颗粒做出反应而释放的。抗体的存在表明存在致病微生物抗原。随着人们对诊断检测重要性的认识不断提高,预计将推动该细分市场的增长。
产品细分分析
到2035年,抗核抗体检测试剂盒市场将占据相当大的收入份额,这得益于其在生命科学研究、药物研发和开发领域的应用日益增长。此外, 自身免疫性疾病药物的不断进步,有望阻止这些可能导致患者死亡的疾病的传播,预计将推动市场的增长。市场分析显示,在欠发达地区或农村地区开展疫苗接种活动的偏远地区,抗核抗体检测试剂盒的使用日益增多,也促进了该细分市场的增长。此外,生物制药行业日益壮大,生产大量用于诊断的试剂盒,也推动了市场的增长。
我们对全球市场的深入分析包括以下几个部分:
技术 |
|
产品 |
|
终端用户 |
|

Vishnu Nair
全球业务发展主管根据您的需求定制此报告 — 联系我们的顾问,获取个性化见解和选项。
抗核抗体测试市场区域分析:
北美市场洞察
到2035年,预计北美地区将占据40.6%的抗核抗体检测市场份额,这主要得益于老年人口的增长和自身免疫性疾病病例的增加。根据美国自身免疫相关疾病协会 (AARDA) 的报告,该地区发现了100多种自身免疫性疾病,而5000万美国人患有某种自身免疫性疾病。此外,北美关节炎病例的增加也预计将推动市场增长。根据美国疾病控制与预防中心发布的报告,预计关节炎患者人数将达到7800万成年人。
亚太市场市场洞察
此外,预计预测期内亚太地区的市场将快速增长,这归因于自身免疫性疾病病例的增加以及老年人口的增长等类似因素。此外,政府在医疗保健领域的举措不断升级也可能是市场增长的主要因素。
抗核抗体测试市场参与者:
- F.霍夫曼-罗氏有限公司
- 公司概况
- 商业策略
- 主要产品
- 财务表现
- 关键绩效指标
- 风险分析
- 近期发展
- 区域影响力
- SWOT分析
- ERBA 诊断公司
- 宙斯科学公司
- 三一生物技术有限公司
- 赛默飞世尔科技公司
- Bio-Rad实验室公司
- 免疫概念公司
- 欧洲免疫医学实验室诊断股份公司
- 抗体公司
- 贝克顿·迪金森公司
最新发展
F. Hoffmann-La Roche Ltd 的处方药 Evrysdi 获得美国食品药品监督管理局 (FDA) 批准,用于治疗两个月以下婴儿的脊髓性肌萎缩症 (SMA)。
美国食品药品监督管理局 (FDA)批准使用由 Zeus Scientific Inc. 开发的数字免疫荧光系统 dIFine。
- Report ID: 4133
- Published Date: Sep 09, 2025
- Report Format: PDF, PPT
- 探索关键市场趋势和洞察的预览
- 查看样本数据表和细分分析
- 体验我们可视化数据呈现的质量
- 评估我们的报告结构和研究方法
- 一窥竞争格局分析
- 了解区域预测的呈现方式
- 评估公司概况与基准分析的深度
- 预览可执行洞察如何支持您的战略
探索真实数据和分析
常见问题 (FAQ)
抗核抗体检测 市场报告范围
版权所有 © 2026 Research Nester。保留所有权利。




